
6.3.3催化剂与反应速率 :1.44y, 例1.Ce4+氧化AsD的反应分两步: 0.56V As(IID) 慢AsV快As() K′=1030 加入少量K紅,可加快反应速度 例2. 2Mn04+5C2042-+16H+=2Mn2++10C02+8H20 开始时反应慢,随着Mn(仙)的产生,反应越来越快. 自动催化反应: 由于生成物本身引起催化作用的反应。 16
16 加入少量KI,可加快反应速度 : 1.44V, 0.56V K = 10 As(III) As(IV) As(V) 慢 快 30 例1.Ce4+氧化As(III)的反应分两步: 2MnO4 - + 5C2O4 2- +16H+ = 2Mn2+ + 10CO2 + 8H2O 开始时反应慢,随着Mn(II)的产生,反应越来越快. 自动催化反应: 由于生成物本身引起催化作用的反应。 例2. 6.3.3 催化剂与反应速率
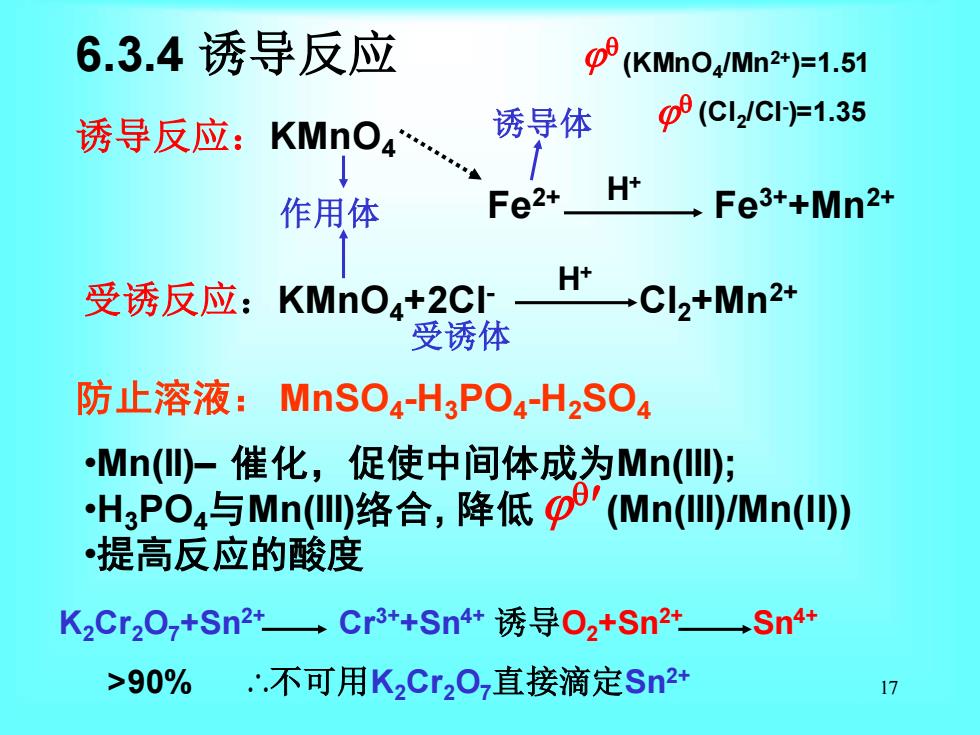
6.3.4诱导反应 (KMnO./Mn2*)=1.51 诱导反应:KMnO4 诱导体 9(Cl2/Cy1.35 H' 作用体 Fe2+ Fe3++Mn2+ 受诱反应:KMnO4+2C H+ 一Cl2+Mn2+ 受诱体 防止溶液:MnSO4-H3PO4-H2SO4 Mn(仙-催化,促使中间体成为Mn(l; H3PO4与Mn(l络合,降低p'(Mn(ID/Mn() 提高反应的酸度 K2Cr20,+Sn2t→Cr3+Sn4+诱导02+Sn2+Sn4+ >90% ∴.不可用K2Cr20,直接滴定Sn2+ 17
17 6.3.4 诱导反应 防止溶液: MnSO4 -H3PO4 -H2SO4 诱导反应:KMnO4 Fe2+ Fe3++Mn2+ 受诱反应:KMnO4+2Cl- Cl2+Mn2+ H+ H+ 诱导体 作用体 受诱体 •Mn(II)– 催化,促使中间体成为Mn(III); •H3PO4与Mn(III)络合, 降低 (Mn(III)/Mn(II)) •提高反应的酸度 K2Cr2O7+Sn2+ Cr3++Sn4+ 诱导O2+Sn2+ Sn4+ >90% ∴不可用K2Cr2O7直接滴定Sn2+ (KMnO4 /Mn2+)=1.51 (Cl2 /Cl- )=1.35

6.4氧化还原滴定曲线及终点的确定 6.4.1氧化还原滴定曲线 以Ce4+滴定Fe2+(均为0.1000moL1)为例: p9(Ce4+1ce3t)=1.4V,p9(fe3+Fe2*)=0.68(1mol-L1Hzs0) 对于滴定的每一点,达平衡时有: o(Fe3*/Fe2+)=o(Ce4*/Ce3*) 滴定前,Fe3+未知,不好计算 sp前,Ce4+未知,按Fe3+Fe2+电对计算 Sp后,Fe2+未知,按Ce4+/Ce3+电对计算 18
18 6.4.1 氧化还原滴定曲线 滴定前,Fe3+未知,不好计算 sp前,Ce4+未知,按Fe3+/Fe2+电对计算 sp后,Fe2+未知,按Ce4+/Ce3+电对计算 3+ 2+ 4+ 3+ (Fe /Fe ) = (Ce /Ce ) 以Ce4+滴定Fe2+(均为0.1000mol·L-1 )为例: 对于滴定的每一点,达平衡时有: , 4+ 3+ 3+ 2+ (Ce /Ce ) =1.44 V (Fe /Fe ) = 0.68 V (1mol·L-1 H2SO4 ) 6.4 氧化还原滴定曲线及终点的确定