
一切物质都具有能量,能量是物质固有的特性。通常, 能量可分为两大类,一类是系统蓄积的能量,如动能、势能 和热力学能,它们都是系统状态的函数。另一类是过程中系 统和环境传递的能量,常见有功和热量,它们就不是状态函 数,而与过程有关。热量是因为温度差别引起的能量传递, 而做功是由势差引起的能量传递。 因此,热和功是两种本质不同且与过程传递方式有关 的能量形式
一切物质都具有能量,能量是物质固有的特性。通常, 能量可分为两大类,一类是系统蓄积的能量,如动能、势能 和热力学能,它们都是系统状态的函数。另一类是过程中系 统和环境传递的能量,常见有功和热量,它们就不是状态函 数,而与过程有关。热量是因为温度差别引起的能量传递, 而做功是由势差引起的能量传递。 因此,热和功是两种本质不同且与过程传递方式有关 的能量形式

热力学第一定律 第一定律的文字表述: (A)能量不生不灭,能量守恒(第一定律本质) (B)第一类永动机不可能造成。 第一定律认为:体系由状态1经任意过程和任意途径变化到 状态2,若在过程中交换了6Q的热,并作了6W的功,则 体系的内能变化为dU=δQ+δW:或者△U=Q+W
热力学第一定律 第一定律的文字表述: (A)能量不生不灭,能量守恒(第一定律本质) (B)第一类永动机不可能造成。 第一定律认为:体系由状态1经任意过程和任意途径变化到 状态2,若在过程中交换了δQ的热,并作了δW的功,则 体系的内能变化为 dU=δQ+δW; 或者△U=Q+W
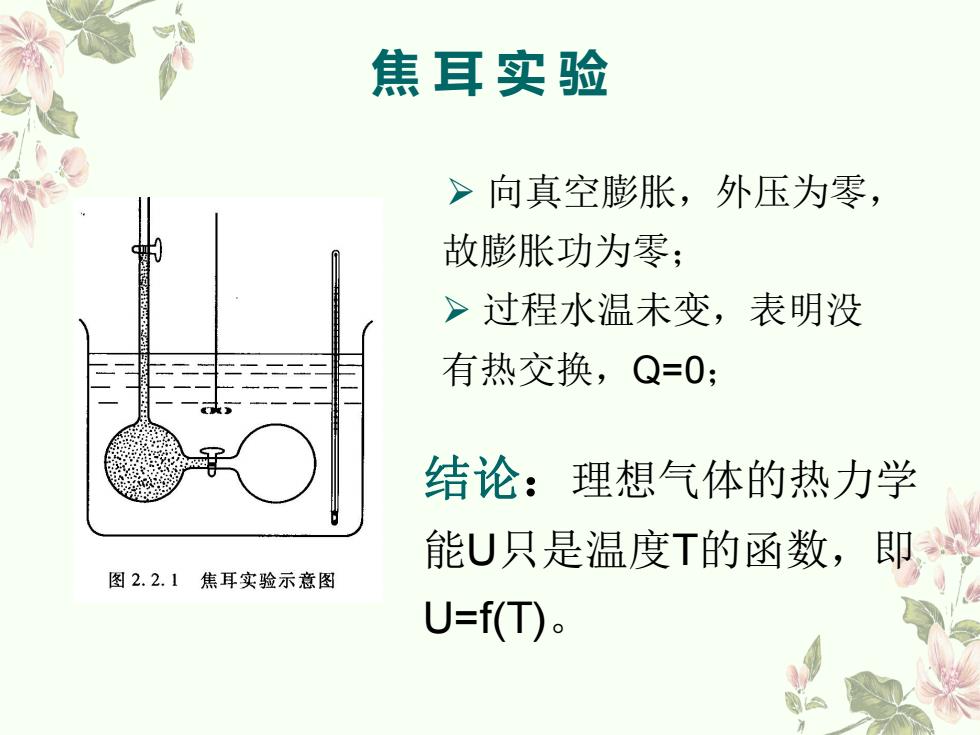
焦耳实验 >向真空膨胀,外压为零, 故膨胀功为零; >过程水温未变,表明没 有热交换,Q=0: 结论:理想气体的热力学 能U只是温度T的函数,即 图2.2.1焦耳实验示意图 U=f(T)
焦 耳 实 验 Ø 向真空膨胀,外压为零, 故膨胀功为零; Ø 过程水温未变,表明没 有热交换,Q=0; 结论:理想气体的热力学 能U只是温度T的函数,即 U=f(T)
例一体系由A态变化到B态,沿途径放热100J, 对体系做功50J,问:1.由A态沿途径1到B态,体 系做功80J,则过程Q值为多少?2.如果体系再由 B态沿途径III回到A态,得到50J的功,体系是吸 热还是放热?Q值是多少? A
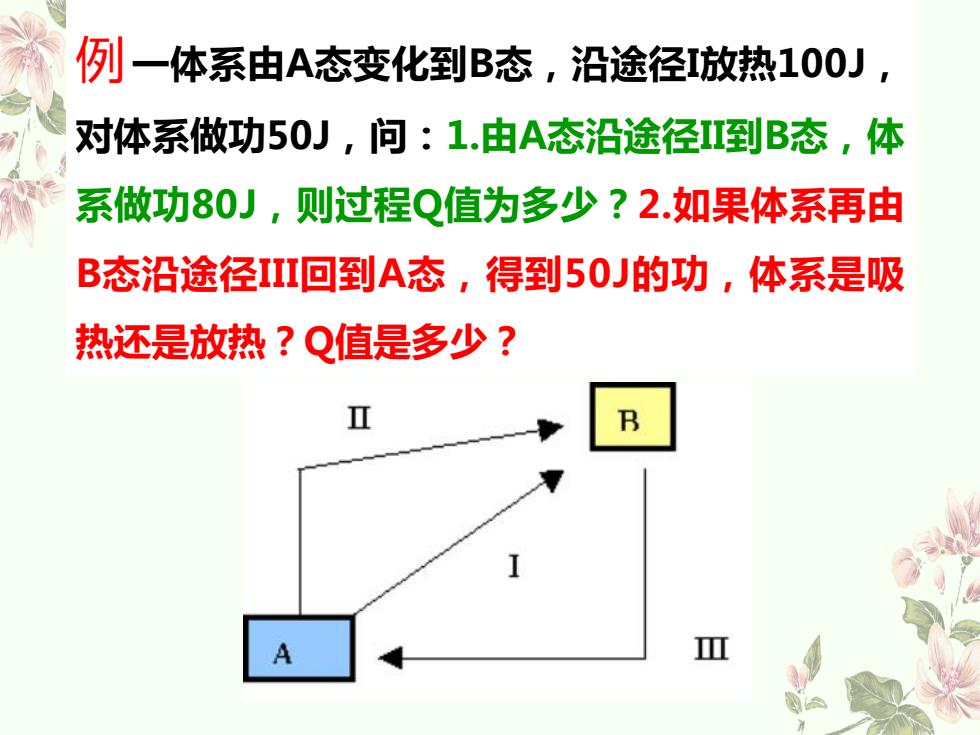
例一体系由A态变化到B态,沿途径I放热100J, 对体系做功50J,问:1.由A态沿途径II到B态,体 系做功80J,则过程Q值为多少?2.如果体系再由 B态沿途径III回到A态,得到50J的功,体系是吸 热还是放热?Q值是多少?

解:途径I,Q=一100J,W=50J (1)△UAB=Q+W=-100+50=-50J ∴.Q=△U+W=-50-(-80)=30J (2)△UBA=-△UAB=50J ∴.Q=△U-W=50-50=0