
化学反应的方向、速率和限度 3.化学反应的吉布斯自由能变 热化学反应方向的判据 1873年,美国化学家Gibbs J.W.引进 了一个新的状态函数一Gibbs函数(也 称Gibbs自由焓或自由焓),用符号G表 示。 将决定某过程的自发性的三个因素:焓 变、熵变和温度,统一起来作为新的判 G晒定章mo1 Gibbs函数的定义式 2009-6-2 26
2009-6-2 26 化学反应的方向、速率和限度 3.化学反应的吉布斯自由能变 — — 热化学反应方向的判据 1873年,美国化学家Gibbs J.W.引进 了一个新的状态函数— — Gibbs函数(也 称Gibbs自由焓或自由焓),用符号G表 示。 将决定某过程的自发性的三个因素:焓 变、熵变和温度,统一起来作为新的判 据。Gibbs函数的定义式为: G=H-TS 单位:kJ·mol-1

化学反应的方向、速率和限度 焓H、嫡S和热力学温度T都是状态 函数,因此Gbbs函数G是一组合的 状态函数。 Gibbs函数有明确的物理意义: a.Gibbsi函数是状态函数 b.Gibbs函数是可利用的能量 c.Gibbs函数变是自发过程的推动力 27 2009-6-2
2009-6-2 27 化学反应的方向、速率和限度 焓H、熵S和热力学温度T都是状态 函数,因此Gibbs函数G是一组合的 状态函数。 Gibbs函数有明确的物理意义: a. Gibbs函数是状态函数 b.Gibbs函数是可利用的能量 c. Gibbs函数变是自发过程的推动力

化学反应的方向、速率和限度 △G是Gibbs函数变(也称Gibbs自由能变) 。 △rGim=△rHm-T△rSm (Gibbs公式) 定义 G=H-TS (1) 摩尔吉布斯自由能变(自由能变)△Gm (2)吉布斯公式△Gm=△Hm-T△Sm 2009-6-2 28
2009-6-2 28 化学反应的方向、速率和限度 △G是Gibbs函数变(也称Gibbs自由能变)。 G H TS rGm rHm T rSm Gibbs 定义 公式 (1)摩尔吉布斯自由能变(自由能变) △rGm (2)吉布斯公式 △rGm =△rHm- T△rSm

化学反应的方向、速率和限度 (3)热化学反应自发过程的判据 等温、等压,封闭体系,不做非体积功, △,Gm<0自发过程,化学反应可正向进行 △,Gm=0平衡状态 △Gm>0非自发过程,化学反应可逆向进行 由△G=△H-T△S可以看出,温度对Gibbs 函数变有明显的影响,而温度对△H和△S的影 响相对较小,在无机化学中一般不予考虑。 2009-6-2 29
2009-6-2 29 化学反应的方向、速率和限度 (3)热化学反应自发过程的判据 等温、等压,封闭体系,不做非体积功, △rGm < 0 自发过程,化学反应可正向进行 △rGm = 0 平衡状态 △rGm > 0 非自发过程,化学反应可逆向进行 由△G = △H- T△S 可以看出,温度对Gibbs 函数变有明显的影响,而温度对△H 和△S的影 响相对较小,在无机化学中一般不予考虑
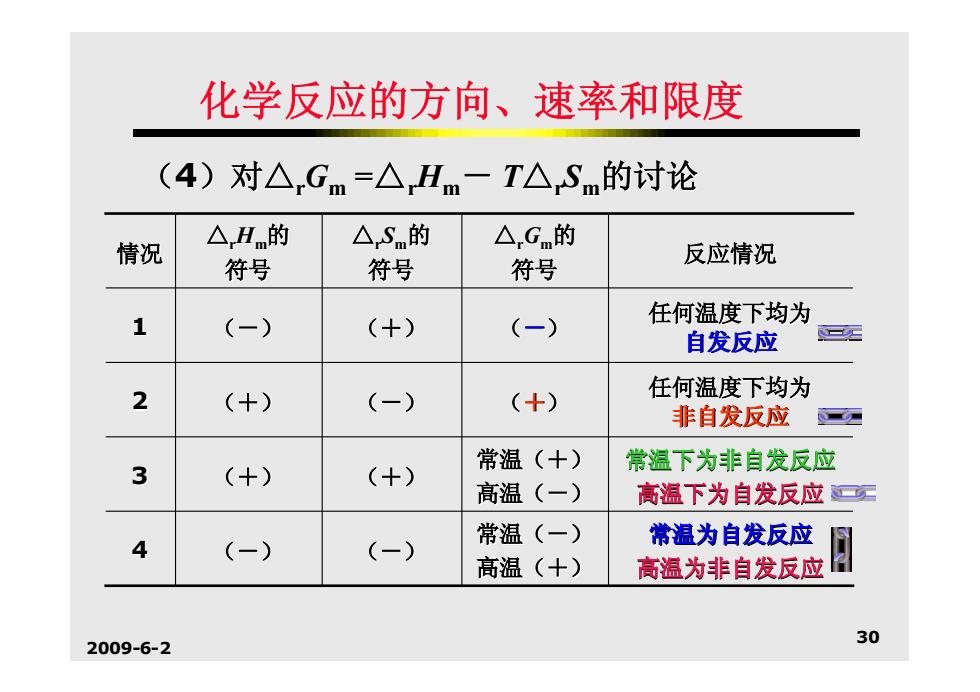
化学反应的方向、速率和限度 (4)对△Gm=△Hm-T△Sm的讨论 △Hm的 △Sm的 △.Gn的 情况 符号 符号 符号 反应情况 1 (-) (+) (-) 任何温度下均为 自发反应 三匹 2 (+) (-) (+) 任何温度下均为 非自发反应 3 (+) (+) 常温(+) 常温下为非自发反应 高温(一) 高温下为自发反应三实 常温(一) 4 (-) (-) 常温为自发反应 高温(十) 高温为非自发反应 2009-6-2 30
2009-6-2 30 化学反应的方向、速率和限度 (4)对△rGm =△rHm- T△rSm的讨论 常温为自发反应 高温为非自发反应 常温(-) 高温(+) 4 (-) (-) 常温下为非自发反应 高温下为自发反应 常温(+) 高温(-) 3 (+) (+) 任何温度下均为 非自发反应 2 (+) (-) (+) 任何温度下均为 自发反应 1 (-) (+) (-) 反应情况 △rGm的 符号 △rSm的 符号 △rHm的 符号 情况