7 5.物质的量 不是质量 万质量守恒? 化学反应物系物质的量可能增大、减小咸者保持不变。 二、可逆过程和不可逆过程 定义:在完成某含有化学反应的过程后,当使过程沿相反 方向进行时,能够使物系和外界完全恢复到原来状态,不留下 任何变化的理想过程。 一切含有化学反应的实际过程都是不可逆的,少数特殊条 件下的化学反应接近可逆。例如? 蓄电池的放电和充电接近可逆; 燃烧反应— 强烈不可逆。 正向反应十 可逆正向反应作出的 有用功最大,其逆向 系统 有用功数值相等 外界 反应时所需输入的有 逆向反应· 用功的绝对值最小。 上游充通大学 2017年4月2 7 SHANGHAI JLAO TONG UNIVERSITY
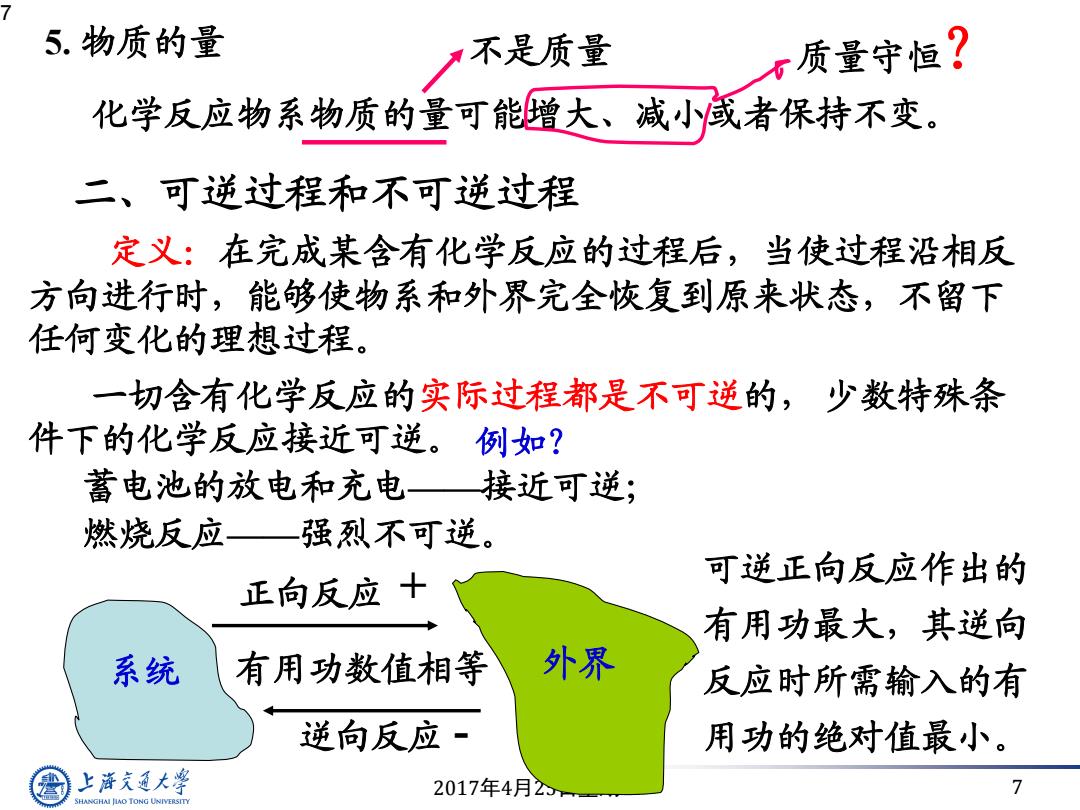
2017年4月25日星期二 7 7 二、可逆过程和不可逆过程 定义:在完成某含有化学反应的过程后,当使过程沿相反 方向进行时,能够使物系和外界完全恢复到原来状态,不留下 任何变化的理想过程。 一切含有化学反应的实际过程都是不可逆的, 少数特殊条 件下的化学反应接近可逆。 蓄电池的放电和充电——接近可逆; 燃烧反应——强烈不可逆。 5. 物质的量 化学反应物系物质的量可能增大、减小或者保持不变。 不是质量 质量守恒? 系统 外界 正向反应 有用功数值相等 逆向反应 + - 可逆正向反应作出的 有用功最大,其逆向 反应时所需输入的有 用功的绝对值最小。 例如?

8 13-2热力学第一定律在化学反应系统的应用 热力学第一定律对于有化学反应的过程也适用; 是对化学过程进行能量平衡分析的理论基础。 一、热力学第一定律解析式 反应热+一Q=U,-U+W (各种形式功的总和) 2=0,-U+W+W (有用功)(体积功) δQ=dU+δW+δW 实际的化学反应过程大量地是在(T,)或(T,P)近似保持不变 的条件下进行的。 上游充通大 2017年4月25日星期二 8 HANGHAI JLAO TONG UNIVERSITY
2017年4月25日星期二 8 8 13-2 热力学第一定律在化学反应系统的应用 热力学第一定律对于有化学反应的过程也适用; 是对化学过程进行能量平衡分析的理论基础。 一、 热力学第一定律解析式 Q U U W 2 1 tot Q U U W W 2 1 u u δ d δ δ Q U W W 反应热 (有用功) (体积功) 实际的化学反应过程大量地是在(T, V)或(T, P)近似保持不变 的条件下进行的。 (各种形式功的总和)