
第6章 实际气体性质及热力学一做关系式 (Behavior of real gases and generalized thermodynamic relationships) 上游充通大学 2018年3月9日 2 SHANGHAI JLAO TONG UNIVERSIT
2018年3月9日 2 第 6 章 实际气体性质及热力学一般关系式 (Behavior of real gases and generalized thermodynamic relationships)

§6-4对应态原理与通用压缩因子图 一,对应态原理(principle of corresponding states) 对比参数(reduced properties)):p,=卫 T T= T 把对比参数P, T Vw 及 27R2T2 a= b= RT R- 64 8Pc 3 T. 代入范氏方程: +加.--m p 可导得 是e这你 范德瓦尔对比态方程 上游气通大学 2018年3月9日 3 HANGHAI JLAO TONG UNIVERSITY
2018年3月9日 3 §6–4 对应态原理与通用压缩因子图 一.对应态原理(principle of corresponding states) m mr c,m r r c c p T V p T V p T V 代入范氏方程: V b RT V a p m m 2 可导得 mr r mr r V T V p 3 1 8 3 2 范德瓦尔对比态方程 对比参数(reduced properties): 2 2 27 8 c,m 64 8 3 r r mr c c c c c c p T V R T RT p V a b R p p T 把对比参数 及

+是}。-=7 讨论: 1)对比态方程中没有物性常数,所以是通用方程; 2)从对比态方程中可看出 相同的p,T下,不同气体的v不同 相同的p,T下,不同气体的v相同,即 各种气体在对应状态下有相同的比体积 对应态原理f,Ty)=0 3)对大量流体研究表明,对应态原理大致是正确的, 若采用“理想对比体积”一Vm', 能提高计算精度。 m m,i,c 其中Vm.,c一临界状态作理想气体计算的摩尔体积 熟 上游充通大学 2018年3月9日 4 HANGHAI JLAO TONG UNIVERSITY
2018年3月9日 4 讨论: 1)对比态方程中没有物性常数,所以是通用方程; 2)从对比态方程中可看出 相同的p,T下,不同气体的v不同 相同的pr,Tr下,不同气体的vr相同,即 各种气体在对应状态下有相同的比体积—— 对应态原理 f(pr ,Tr ,vr )=0 3)对大量流体研究表明,对应态原理大致是正确的, 若采用“理想对比体积”—Vm ',能提高计算精度。 m i c m m V V V , , ' 其中 Vm,i,c 临界状态作理想气体计算的摩尔体积 mr r mr r V T V p 3 1 8 3 2
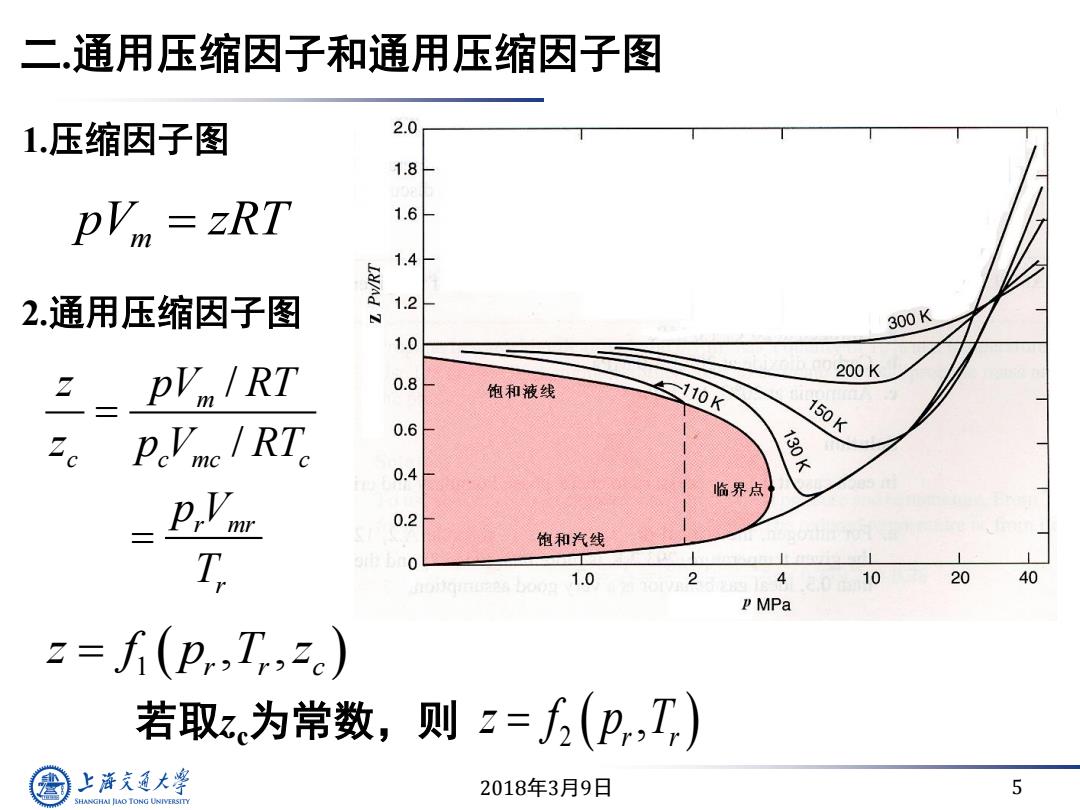
二.通用压缩因子和通用压缩因子图 1.压缩因子图 2.0 1.8 pVm zRT 1.6 1.4- 2.通用压缩因子图 人 1. N 300K 1.0 之=pV/RT 200K 0.8 饱和液线 110K PoVmnc RT 0.6 150K 130K 0.4- 临界点 0.2 饱和汽线 T 0 1.0 4 0 10 20 40 P MPa =f(p:T,=) 若取z为常数,则z=(p,T,) 上游充通大学 2018年3月9日 5 SHANGHAI JLAO TONG UNIVERSITY
2018年3月9日 5 二.通用压缩因子和通用压缩因子图 m pV zRT 2.通用压缩因子图 / / m c c mc c r mr r z pV RT z p V RT p V T 若取zc为常数,则 2 , r r z f p T 1.压缩因子图 z f p T z 1 r r c , ,
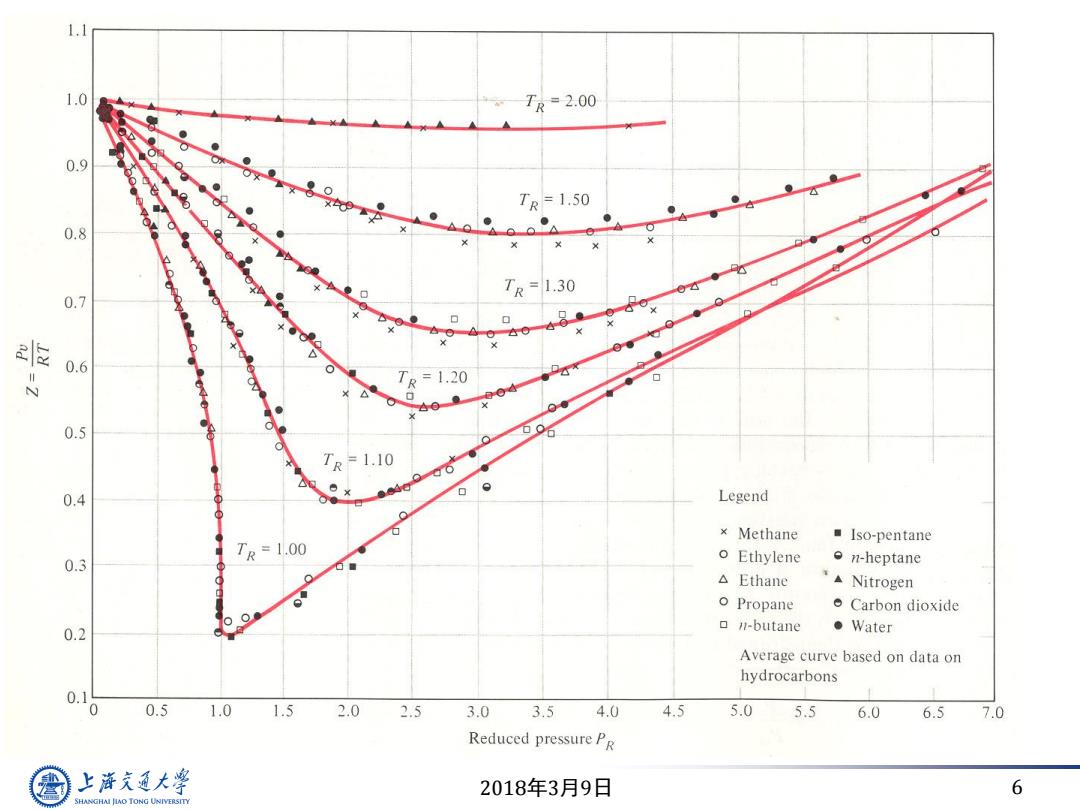
1.0 TR=2.00 0.9 TR=1.50 0.8 TR=1.30 0.7 e 0.6 TR=1.20 0.5 ● TR=1.10 0.4 Legend × Methane Iso-pentane Tr=1.00 O 0.3 Ethylene o n-heptane △Ethane Nitrogen o Propane Carbon dioxide 0.2 ▣-butane ● Water Average curve based on data on hydrocarbons 0.1 0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 6.5 7.0 Reduced pressure PR 图 上文通大学 2018年3月9日 6 SHANGHAI JIAO TONG UNIVERSITY
2018年3月9日 6