难点:常见的核反应类型及核反应的表示 4.教学建议: 自学 第十四章无机化学与生态环境 1.基本内容 生命元素种类及其生物功能:环境污染类型与防治措施:工业“三废”的治理:绿色化学 概念。 2.教学基本要求: 了解:生命元素种类及其生物功能:污染治理:绿色化学 3.教学重点难点: 重点:生命元素种类:污染的治理:绿色化学的中心内容 难点:生命元素的生物功能 4.教学建议: 自学 四、教学环节与学时分配 其 课外辅导 教学内容 备注 时 讲课实验上机其他 课外实 无机化学中的计量关系 化竿反应的万向、 与限2 酸碱反应 4 沉及应 5 氧化还原反 6原子结构和元素周期性 7共价镀与分子的结构 8 配位化合物 9 自学 10 过渡元素(1) 自字 11 过发元素《2 自宇 12 系与锕系元素 13 化 与放射化学简介 14 无机化学与生态环境 自学 五、学中应注意的问题 六、实验内容: 见《无机化学C》课程实验大纲 七、考核方式:
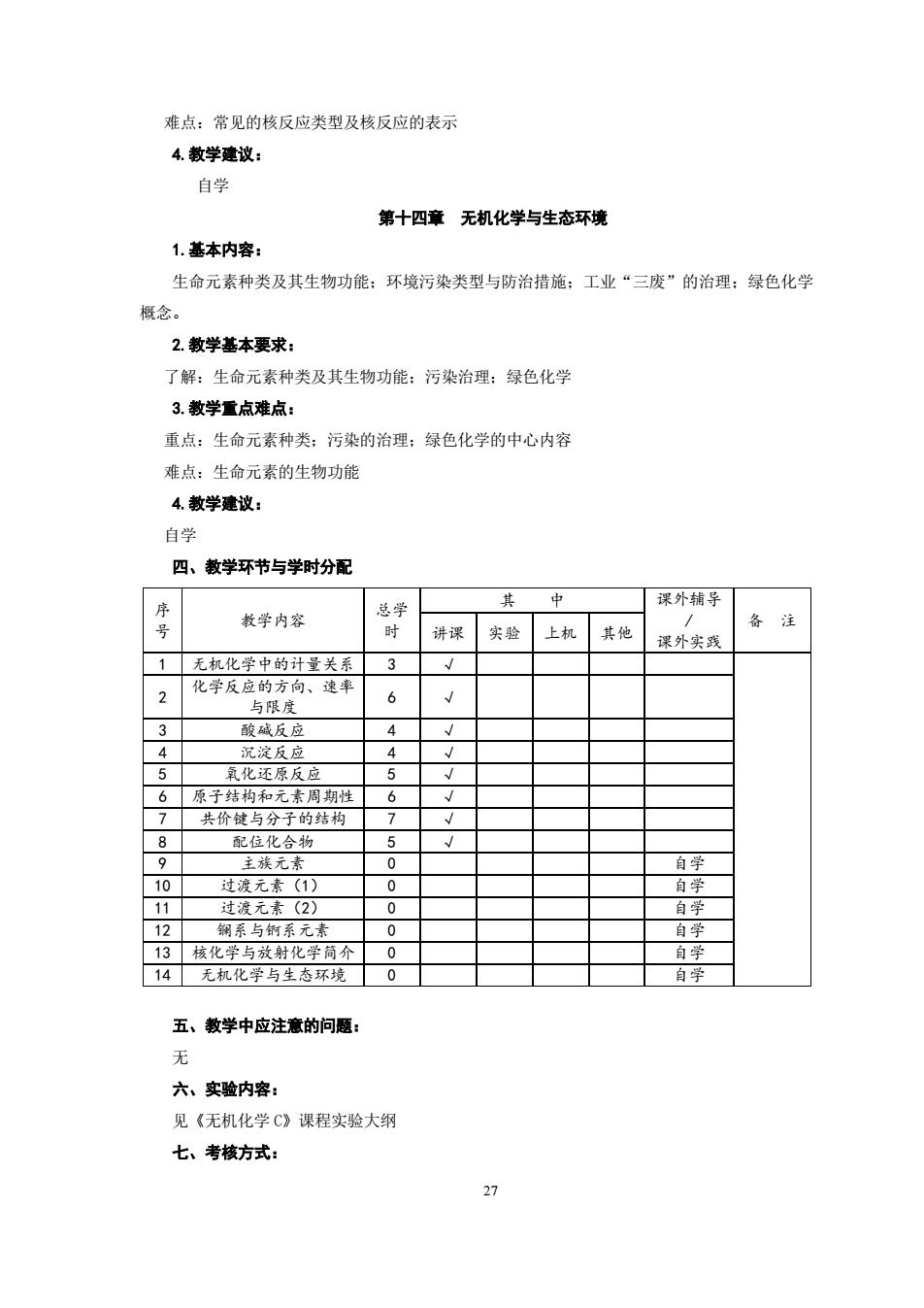
27 难点:常见的核反应类型及核反应的表示 4.教学建议: 自学 第十四章 无机化学与生态环境 1.基本内容: 生命元素种类及其生物功能;环境污染类型与防治措施;工业“三废”的治理;绿色化学 概念。 2.教学基本要求: 了解:生命元素种类及其生物功能;污染治理;绿色化学 3.教学重点难点: 重点:生命元素种类;污染的治理;绿色化学的中心内容 难点:生命元素的生物功能 4.教学建议: 自学 四、教学环节与学时分配 序 号 教学内容 总学 时 其 中 课外辅导 / 课外实践 备 注 讲课 实验 上机 其他 1 无机化学中的计量关系 3 √ 2 化学反应的方向、速率 与限度 6 √ 3 酸碱反应 4 √ 4 沉淀反应 4 √ 5 氧化还原反应 5 √ 6 原子结构和元素周期性 6 √ 7 共价键与分子的结构 7 √ 8 配位化合物 5 √ 9 主族元素 0 自学 10 过渡元素(1) 0 自学 11 过渡元素(2) 0 自学 12 镧系与锕系元素 0 自学 13 核化学与放射化学简介 0 自学 14 无机化学与生态环境 0 自学 五、教学中应注意的问题: 无 六、实验内容: 见《无机化学 C》课程实验大纲 七、考核方式:

见《无机化学C》课程考试大纸 八、教材及主要参考书: 1、选用教材: 《无机化学》第二版,周德风、袁亚莉主编,华中科技大学出版社,2014年 2、主要参考书: 《无机化学》第二版,谢吉民主编,人民卫生出版社,2013年 九、教改说明及其他: 无。 执笔人:王平系室审核人:肖锡林 28
28 见《无机化学 C》课程考试大纲 八、教材及主要参考书: 1、选用教材: 《无机化学》第二版,周德凤、袁亚莉主编,华中科技大学出版社,2014 年 2、主要参考书: 《无机化学》第二版,谢吉民主编,人民卫生出版社,2013 年 九、教改说明及其他: 无。 执笔人:王平 系室审核人:肖锡林

《无机化学C》课程考试大纲 Inorganic Chemistry C 课程编号:130805025 总学时数:40学时 学分:2.5 一、考试对象: 修完本课程规定的各专业学生。 二、考试目的 本课程考试目的是使学生了解现代无机化学的基本理论,具备必要的化学基本知识和一定 的基本技能,为后续课程学习、将来的工作实践和掌握新的科学技术打下必要的化学基础。 三、考试要求 本课程是一门专业基础课,要求学生掌握物质结构的基础理论、化学反应的基本原理、溶 液的性质、化学平衡及元素化学的基本知识:培养学生具有独立思考、分析和解决问题的能力。 四、考试内容与要求 第一章:无机化学中的计量关系80分值 1考试内容:溶液的各种组成标度,理性气体状态方程,化学反应的质量关系和能量关系 化学计量数与反应进度、反应热与反应焓变及其相关计算。 2.考试要求:能进行溶液各种组成标度之间的换算,理性气体状态方程的计算,热化学方程 式的正确写法,以及化学反应格变相关计算。 第二章:化学反应的方向、速率与限度15-18分值 1考试内容:状态函数的概念,反应熵变、吉布斯自由能变△rGm的计算:化学反应的方向 的判定:平衡常数的写法:化学平衡的移动:反应速率的意义及速*方程表达式:浓度、温度 与催化剂对化学反应速率的影响,化学反应速率理论。 2.考试要求:进行化学反应的方向的判定、化学平衡常数的计算、和术语、以及运用化学反 应速率理论判定浓度、温度与催化剂对化学反应速率的影响。 第三章:酸碱反应 12-15分值 1考试内容:水溶液中的质子转移平衡及有关计算,强电解质理论,酸碱理论:缓冲溶液的 基本概念,pH值计算近似计算。 2.考试要求:能进行弱酸弱碱及缓冲溶液有关pH的计算:考察影响pH的因素。 第四章:沉淀反应 12-15分值 1.考试内容:溶度积规则及有关计算:稀释效应、同离子效应、盐效应及对弱电解质的电离 平衡的影响:溶度积Ksp,溶度积规则。 2.考试要求:能进行溶度积与溶解度相互运算,能进行沉淀反应的相关计算。 了解:分步沉淀及转化。 29
29 《无机化学 C》课程考试大纲 Inorganic Chemistry C 课程编号:130805025 总学时数:40 学时 学分:2.5 一、考试对象: 修完本课程规定的各专业学生。 二、考试目的 本课程考试目的是使学生了解现代无机化学的基本理论,具备必要的化学基本知识和一定 的基本技能,为后续课程学习、将来的工作实践和掌握新的科学技术打下必要的化学基础。 三、考试要求 本课程是一门专业基础课,要求学生掌握物质结构的基础理论、化学反应的基本原理、溶 液的性质、化学平衡及元素化学的基本知识;培养学生具有独立思考、分析和解决问题的能力。 四、考试内容与要求 第一章:无机化学中的计量关系 8-10 分值 1.考试内容:溶液的各种组成标度,理性气体状态方程,化学反应的质量关系和能量关系, 化学计量数与反应进度、反应热与反应焓变及其相关计算。 2.考试要求:能进行溶液各种组成标度之间的换算,理性气体状态方程的计算,热化学方程 式的正确写法,以及化学反应焓变相关计算。 第二章:化学反应的方向、速率与限度 15-18 分值 1.考试内容:状态函数的概念,反应熵变、吉布斯自由能变 ΔrGm 的计算;化学反应的方向 的判定;平衡常数的写法;化学平衡的移动;反应速率的意义及速率方程表达式;浓度、温度 与催化剂对化学反应速率的影响,化学反应速率理论。 2. 考试要求:进行化学反应的方向的判定、化学平衡常数的计算、和术语、以及运用化学反 应速率理论判定浓度、温度与催化剂对化学反应速率的影响。 第三章:酸碱反应 12-15 分值 1.考试内容:水溶液中的质子转移平衡及有关计算,强电解质理论,酸碱理论;缓冲溶液的 基本概念,pH 值计算近似计算。 2.考试要求:能进行弱酸弱碱及缓冲溶液有关 pH 的计算;考察影响 pH 的因素。 第四章:沉淀反应 12-15 分值 1.考试内容:溶度积规则及有关计算;稀释效应、同离子效应、盐效应及对弱电解质的电离 平衡的影响;溶度积 Ksp,溶度积规则。 2.考试要求:能进行溶度积与溶解度相互运算,能进行沉淀反应的相关计算。 了解:分步沉淀及转化

第五章:氧化还原反应15-18分值 1考试内容:氧化还原方程式配平,原电池的表达方式,电极电势及其影响因素,判断氧化 还原性的强弱,判断氧化还原反应的方向及平衡常数的计算,N©mt方程的应用,元素电势图 的应用。 2.考试要求:原电池的写法,能判断标准态下和非标准状态下氧化还原反应的方向,己经进 行氧化还原反应的方向的判定及平衡常数的计算。 第六章:原子结构和元素周期性12-15分值 1考试内容:原子核外电子的排布规律,电子排布式和轨道式的书写,量子数概念及取值规 则,元素性质的周期性与原子结构的关系。 2.考试要求:能进行电子排布式和轨道式的书写,能根据元素的电子组态确定它在元素周期 表中的位置,元素性质的周期性变化规律。 第七章:共价键与分子的结构10-15分值 1考试内容:共价键的特征,杂化轨道理论,常见分子的构型,分子间力(取向力、诱导力、 色散力)和氢键。 2.考试要求:能用杂化轨道理论判定常见分子构型,能判定分子间力及氢键,以及对物 理性质的影响。 第八章:配位化合物 10-15分值 1考试内容:配位化合物的基本概念,配合物的组成和命名方法,配合物分子构型的判定 配位平衡移动的主要因素及相关计算 2考试要求:能进行配合物的命名及书写,常见配合物分子构型,以及配位平衡的相关计算。 第九章:主族元素 不作为考试内容 第十章:过渡元素(1) 不作为考试内容 第十一章:过渡元素(2) 不作为考试内容 第十二章:镧系与锕系元素 不作为考试内容 第十三章:核化学与放射化学简介 不作为考试内容 第十四章:无机化学与生态环境 不作为考试内容 五、考试方式及时间 闭卷:100分钟 六、考试愿型结构及分值分布: 选择题:25^30%:判断愿:1015%:填空题:2030%: 简答题:1015%:计算题:2535% 七、成绩综合评定方法: 学生最后总成绩由平时成绩30%平时成绩(到课率10%+课堂表现10%+课后作业10%) +70%考试成绩的总和确定。 30
30 第五章:氧化还原反应 15-18 分值 1.考试内容:氧化还原方程式配平,原电池的表达方式,电极电势及其影响因素,判断氧化 还原性的强弱,判断氧化还原反应的方向及平衡常数的计算,Nernst 方程的应用,元素电势图 的应用。 2.考试要求:原电池的写法,能判断标准态下和非标准状态下氧化还原反应的方向,已经进 行氧化还原反应的方向的判定及平衡常数的计算。 第六章:原子结构和元素周期性 12-15 分值 1.考试内容:原子核外电子的排布规律,电子排布式和轨道式的书写,量子数概念及取值规 则,元素性质的周期性与原子结构的关系。 2.考试要求:能进行电子排布式和轨道式的书写,能根据元素的电子组态确定它在元素周期 表中的位置,元素性质的周期性变化规律。 第七章:共价键与分子的结构 10-15 分值 1.考试内容:共价键的特征,杂化轨道理论,常见分子的构型,分子间力(取向力、诱导力、 色散力)和氢键。 2.考试要求:能用杂化轨道理论判定常见分子构型,能判定分子间力及氢键,以及对物 理性质的影响。 第八章:配位化合物 10-15 分值 1.考试内容:配位化合物的基本概念,配合物的组成和命名方法,配合物分子构型的判定, 配位平衡移动的主要因素及相关计算 2.考试要求:能进行配合物的命名及书写,常见配合物分子构型,以及配位平衡的相关计算。 第九章:主族元素 不作为考试内容 第十章:过渡元素(1) 不作为考试内容 第十一章:过渡元素(2) 不作为考试内容 第十二章:镧系与锕系元素 不作为考试内容 第十三章:核化学与放射化学简介 不作为考试内容 第十四章:无机化学与生态环境 不作为考试内容 五、考试方式及时间 闭卷;100 分钟 六、考试题型结构及分值分布: 选择题:25~30%;判断题:10~15%;填空题:20~30%; 简答题:10~15%;计算题:25~35% 七、成绩综合评定方法: 学生最后总成绩由平时成绩 30% 平时成绩(到课率 10% + 课堂表现 10% +课后作业 10%) + 70% 考试成绩的总和确定

八、教材及主要参考书: 1、选用教材: 《无机化学》第二版,周德风、袁亚莉主编,华中科技大学出版社,2014年 2、主要参考书: 《无机化学》袁亚莉、周德风主编,华中科技大学出版社,2007年 《无机化学》第二版,谢吉民主编,人民卫生出版社,2013年 执笔人:王平系室审核人:肖锡林 3
31 八、教材及主要参考书: 1、选用教材: 《无机化学》第二版,周德凤、袁亚莉主编,华中科技大学出版社,2014 年 2、主要参考书: 《无机化学》袁亚莉、周德凤主编,华中科技大学出版社,2007 年 《无机化学》第二版,谢吉民主编,人民卫生出版社,2013 年 执笔人:王平 系室审核人:肖锡林