半导体的电子结构 及AU IUNC NYC0eN 原子的构成: 电子云2个电子(-Z) 质子 中子 (Z个、+Z) (A-Z个) 1.构成原子核的质子的个数称为原子序数乙, 质量数:质子数+中子数 质子的个数和中子的个数之和称为质量数A。 一般情况下,Z和A分别缀写在元素符号的左 下角和左上角。 ew 2.原子的化学属性主要由电子云决定。 原子序数:质子数
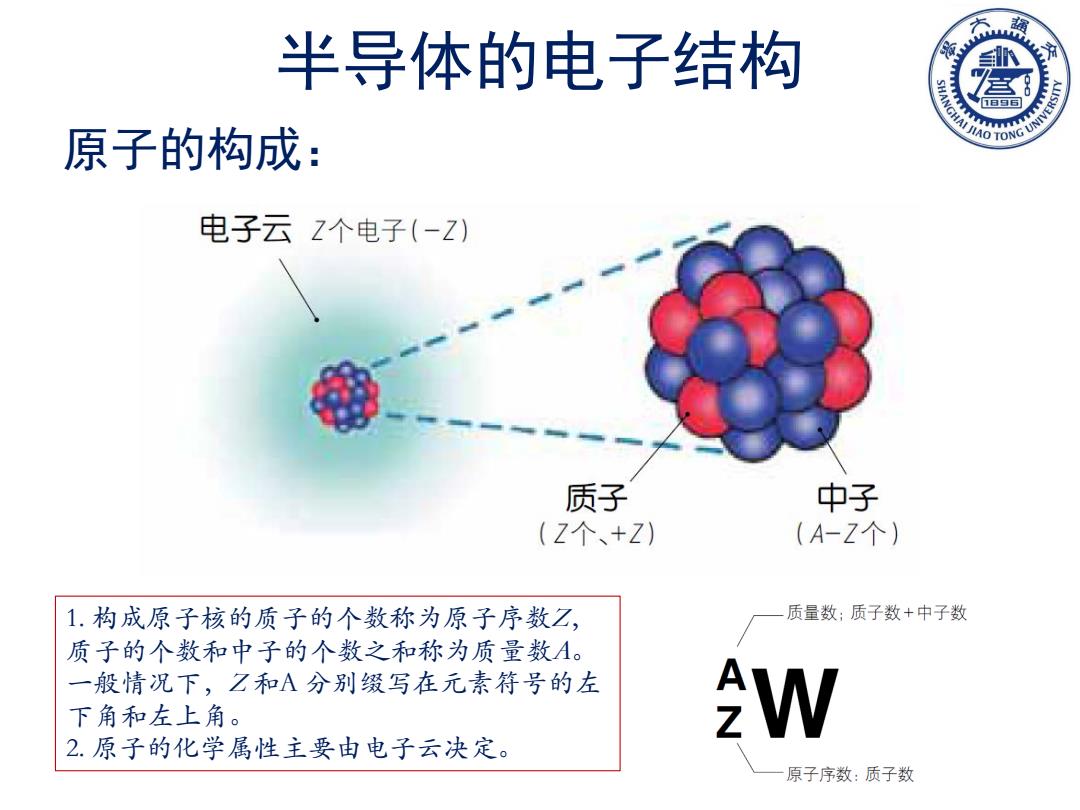
半导体的电子结构 原子的构成: 1. 构成原子核的质子的个数称为原子序数Z, 质子的个数和中子的个数之和称为质量数A。 一般情况下,Z 和A 分别缀写在元素符号的左 下角和左上角。 2. 原子的化学属性主要由电子云决定
能带理论 ·单个原子中的电子在绕核运动时,在各个轨 ANGHAI JIAO TONG UNIVERSTN 道上的电子都各自具有特定的能量; 电子能量E ·越靠近核的轨道,电子能量越低; ·能量最小原理:电子总是优先占有最低能级; 导带 价电子所占据的能带称为价带; 禁带(Eg)中不存在为电子所占据的能级;B, 禁带 导带:自由电子所能占据的能级; 价带 ·Eg其值与半导体的材料及其所处的温度等因 素有关。T=300K时,硅的Eg=1.1eV;锗的 Eg=0.72eV 重叠 价电子的能带图 能量 导带 费米能级 禁带 价带 上充通大粤 金属 半导体 绝缘体
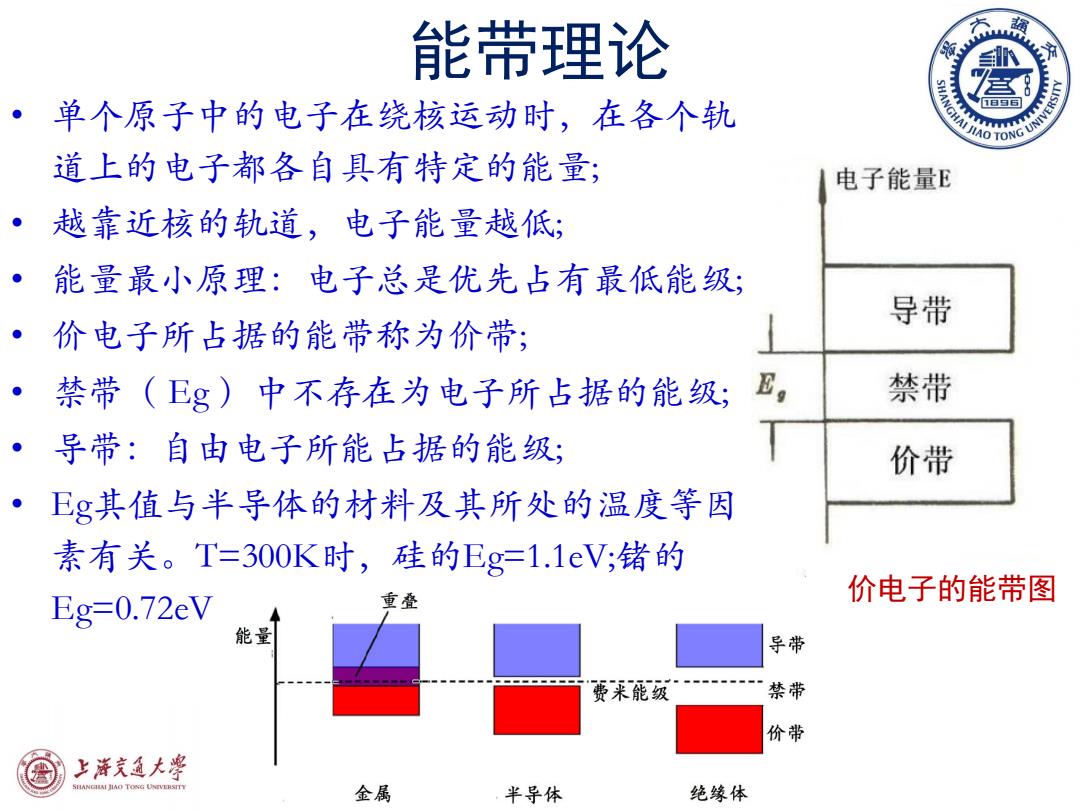
能带理论 • 单个原子中的电子在绕核运动时,在各个轨 道上的电子都各自具有特定的能量; • 越靠近核的轨道,电子能量越低; • 能量最小原理:电子总是优先占有最低能级; • 价电子所占据的能带称为价带; • 禁带( Eg )中不存在为电子所占据的能级; • 导带:自由电子所能占据的能级; • Eg其值与半导体的材料及其所处的温度等因 素有关。T=300K时,硅的Eg=1.1eV;锗的 Eg=0.72eV。 价电子的能带图

半导体的电子结构 ·物质的导电性能决定于原子结构。 ·导体一般为低价元素,它们的最外层电子极易挣脱原子核的束 缚成为自由电子,在外电场的作用下产生定向移动,形成电流。 ·高价元素(如惰性气体)或高分子物质(如橡胶),它们的最外层电 子受原子核束缚力很强,成为绝缘体。 ·硅(Si)和锗(Ge)均为四价元素,它 们的最外层电子性质介于二者之 间—半导体。将纯净的半导体 共价键 经过一定的工艺过程制成单晶体, 即为本征半导体。晶体中的原子 在空间形成排列整齐的点阵,相 邻的原子形成共价键
半导体的电子结构 • 物质的导电性能决定于原子结构。 • 导体一般为低价元素,它们的最外层电子极易挣脱原子核的束 缚成为自由电子,在外电场的作用下产生定向移动,形成电流。 • 高价元素(如惰性气体)或高分子物质(如橡胶),它们的最外层电 子受原子核束缚力很强,成为绝缘体。 • 硅(Si)和锗(Ge)均为四价元素,它 们的最外层电子性质介于二者之 间——半导体。将纯净的半导体 经过一定的工艺过程制成单晶体, 即为本征半导体。晶体中的原子 在空间形成排列整齐的点阵,相 邻的原子形成共价键
Si 在 IA 元素周期表 0 电子层 原子 He 氢 元素符号,红色 15 IIA 序数 92 U 指放射性元素 非金属 金属 VA VIA 1s2 1008 4003 3 Li 4 Be 元素名 铀 外图电子层排布, B 7N 10 Ne 2 锂 铍 称注* 括号指可能的电子 硼 碳 氮 氧 氟 氖 2s 252 的是人 5f6d17s2 层排布 过渡元素 2s22p 2s22D 2s22p3 2s22p 2s2203 2s22p9 L 6941 9.012 造元素 10.81 1201 14.01 16.00 1900 2018 11 Na 12 Mo 238.0 相对原子质量 13 Al 4S 16 S Ar 3 钠 镁 铝 硅 磷 硫 氯 氩 M 3s 3s2 B IVB VB B wB VⅢ ⅡB 3s23p 3s23p2 3s3p 3s3p 3s23p 3s3p L 22.99 24.31 26.98 2809 3097 32.07 3545 39.95 K 19K 20 Ca 21 Sc 22T中 23V 24 Cr 25 Mn 26 Fe 27 Co 28 Ni 29 Cu 30 Zn 31 Ga 32 Ge As Se 酒BF 38 Kr 钾 钙 钪 钛 钒 铬 锰 铁 钴 镍 铜 锌 镓 锗 砷 硒 溴 氪 M 4s 4s 3d'4s 3d24s2 3d4s2 3d4s 3d54s2 3d4s2 3d74s2 3d4s2 3d104s 3d104s 4s24p 4s24p2 4s24p 4s24p 4s24p 4s24p L 39.10 40.08 44.96 4787 50.94 52.00 54.94 5585 58.93 58.69 63.55 6539 69.72 72.61 74.92 78.96 79.90 8380 K 37R6 38 Sr 39Y 40 Zr 41 Nb 42 Mol 43■TG 44 Ru 45 Rh 46 Pdl 47 Ag 48 Cd 491n 50 Sn 51 Sb Xe 0 5 铷 锶 钇 锆 铌 钥 锝 钉 铑 钯 银 镉 铟 锡 锑 碲 碘 氙 M 5s 4d'5s2 4d25s2 4d5s 4d5s 4d5s2 4d75s 4d5s 4d10 4d105s 4d105s 5s25p 5s25p2 5s25p 5s25p 5s25p 5s25p L 85.47 87.62 88.91 91.22 92.91 95.94 f99 101.1 102.9 106.4 107.9 112.4 114.8 118.7 121.8 127.6 1269 1313 K 55 Cs 56 Ba 57-71 72 Hf 73 Ta 74W 75 Re 76 Os 77 Ir 78 Pt 79 Au 80 Hg 81 TI 82Pb83B1 84P0 西AI 8 Rn 6 铯 钡 La-Lu 铪 钽 钨 铼 锇 铱 铂 金 汞 铊 铅 铋 钋 砹 氨 N 65 6s 镧系 5d26s2 5d6s2 5d6s2 5d6s2 5d6s2 5d6s2 5d36s 5d106s 5d6s2 6s26p 6s26p2 6s26p3 6s26p 6s26p 6s26p9 L 132.9 137.3 178.5 180.9 183.8 186.2 190.2 192.2 195.1 197.0 200.6 204.4 207.2 209.0 2091 210 222 K 87 Fr 88 Ra 89103 104Rt 105Db 106Sg 107Bh108Hs 109Mt 0 Ds 111 Rg 112 Cn 113 Uut 114 FI 115 Uup 16 Lv 17 Uus 18Uu0 钫 镭 Ac-Lr 卢* 杜* 喜* 波* 黑* 麦冰 达* 仑* 哥* 鈇* 米 鉝* 7s 锕系 (6d27s3 6d37s3 6d7s2)6d7s2) 6d7s3 2231 226.0 2611 [262 2631 262 2651 266 269 [272 285 284 [2891 288 293 2941 57 La 58 Ce 59 Pr 60 Nd 61 Pm 62 Sm 63 Eu64 Gd 65 66 DY 67 Ho 68 Er 69 70 Yb 71 Lu 镧 铈 镨 钕 钷 钐 铕 钆 铽 镝 钬 铒 铥 镱 镥 1.相对原子质量录自19 系 5d'6s2 4f6s2 46s2 4f6s2 46s2 4f6s24f5d'6s2 4P6s2 4f6s2 4f16s2 4f26s2 416s2 416s2P5d6s2 年国际原子量表,并全部取 138.9 140.1 1409 144.2 [147 150.4152.0 157.3 1589 1625 164.9 1673 168.9 173.0 175.0 有效数字。 89 Ac 90 Th 91 Pa 92 U 93 Np 94 Pu 95 Am96 Cm97 Bk 98 Cf 99 Es 100 Fm 101 Md 102 No 103 Lr 2.相对原子质量加括号 锕 钍 镤 铀 镎 钚 镅* 锔* 锫* 锎* 锿* 镄* 钔* 锘* 铹 为放射性元素的半衰期最长 系 6d7s2 6d27s25f6d'7s256d'7s25r6d'7s2 5P7s2 5f7s25f6s'782 5P7s25f107s2 5f17s2 5f27s2 (5f137s5f7s356d7 同位素的质量数
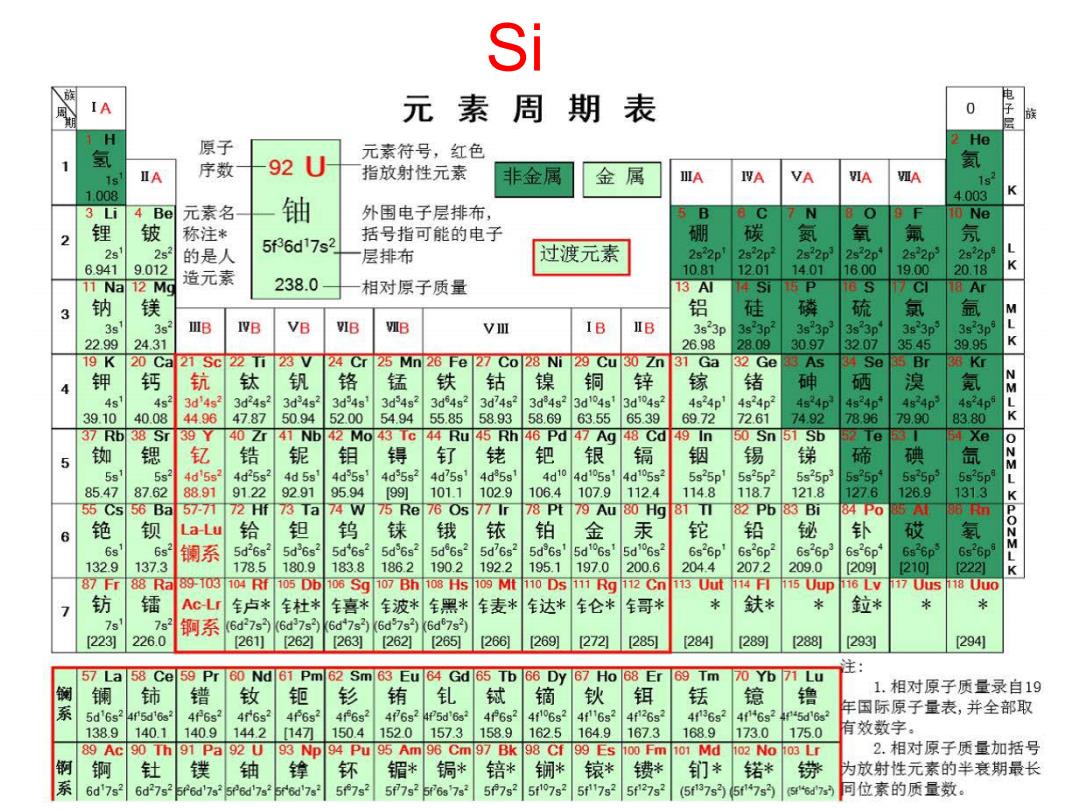
Si

大了 太可了 硅$i,旧称矽。 从那以后约莫过了 桂失败了。 黄金搭档分离 克和泰纳尔这对 三年盖·8花 在地壳中,它是第二丰 富的元素(26.4%) 极少以单质的形式存在。 出了单质社 氟化桂,成功分离 他通过金属甲还原 C177018484l 回东利与斯 端典化学室 广泛存在于岩石、砂砾、 尘土之中 建了一个幸福家庭 出多岁的女性结唱,组 晚年他与一位比他小 元素, 字母表示各种化学 出了用现在的拉丁 回采利马斯最先提
• 硅Si,旧称矽。 • 在地壳中,它是第二丰 富的元素(26.4%)。 • 极少以单质的形式存在。 • 广泛存在于岩石、砂砾、 尘土之中