2.1化学反应的方向和吉布斯函数变 各晷晷光 HCI(g)+NH3 (gNHCI(S) △H6(298.15K)=-176.9kJ·mo1-1 △Sme(298.15K)=-284.3J·mo1-1·K-1 常温为自发反应 0 高温为非自发反应 自发转化温度T: T<△Hm0/△Sm6=622K 20252/15 下页 21
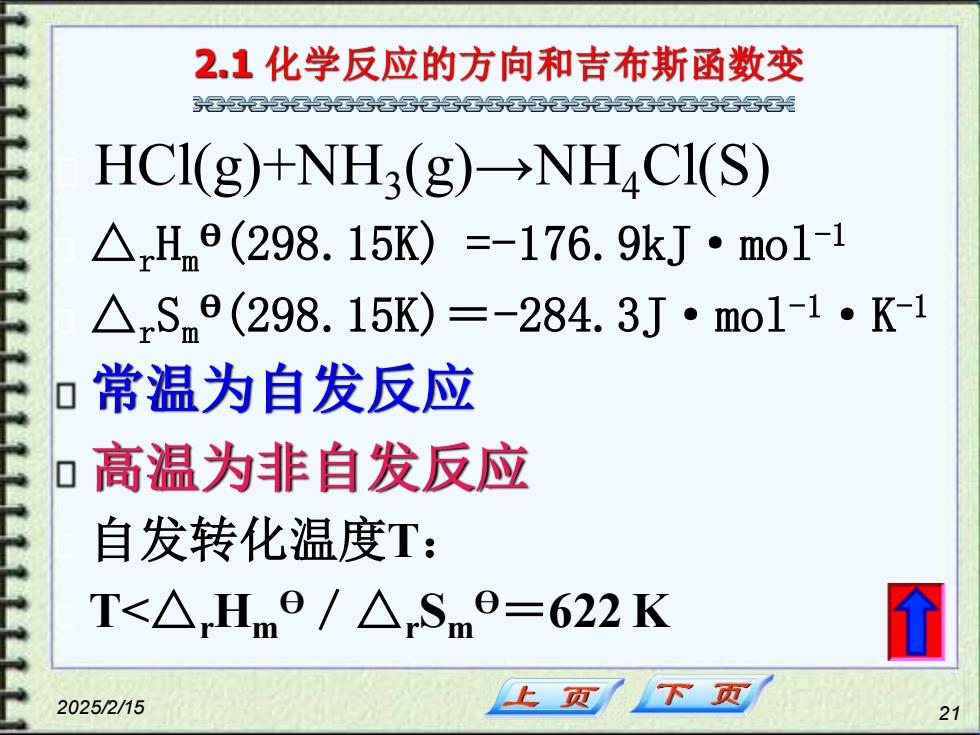
2025/2/15 21 2.1 化学反应的方向和吉布斯函数变 HCl(g)+NH3 (g)→NH4Cl(S) △rHm Ө(298.15K) =-176.9kJ·mol-1 △rSm Ө(298.15K)=-284.3J·mol-1·K-1 常温为自发反应 高温为非自发反应 自发转化温度T: T<△rHm Ө/△rSm Ө=622 K

2.1化学反应的方向和吉布斯函数变 兴兴兴兴名 2.△rGm与△rGmo的关系 任意状态下,化学反应: aA(g)+bB(g)=gG(g)+dD(g) △rGm=△rG9+RTn {PIP}8.{P,/p} {P4/P}.{Pa/p) 2025/2/15 上页 下页 22
2025/2/15 22 2.1 化学反应的方向和吉布斯函数变 2. △rGm与△rGmӨ的关系 任意状态下,化学反应: aA(g)+bB(g) =gG(g) + dD(g) b B a A d D g G m P P P P P P P P rGm rG RT { / } { / } { / } { / } ln = +

2.1化学反应的方向和吉布斯函数变 各晷各晷光 热力学等温方程式: △.Gm=△.G9m+RTInQ 2 反应商 [p(G)/p°][pD)/p°] [p(A)/p°][p(B)/p°] 2025/2/15 上页 下页 23
2025/2/15 23 2.1 化学反应的方向和吉布斯函数变 热力学等温方程式: △rGm =△rGӨ m+ RTlnQ Q ——反应商 ( ) ( ) ( ) ( ) a b g d [ A / ] [ B / ] [ G / ] [ D / ] p p p p p p p p Q =

2.1化学反应的方向和吉布斯函数变 兴名客名各名写名云云名名国云兴云云兴 对于水溶液中的离子反应: aA(aq)+bB(aq)=gG(aq)+dD(aq) Lc(G)/clc(D)/c [c(A)/c [c(B)/c] 2025/2/15 上页 下页 24
2025/2/15 24 2.1 化学反应的方向和吉布斯函数变 对于水溶液中的离子反应 : aA(aq)+bB(aq)=gG(aq)+dD(aq) ( ) ( ) ( ) ( ) a b g d [ A / ] [ B / ] [ G / ] [ D / ] c c c c c c c c Q =

2.1化学反应的方向和吉布斯函数变 各晷晷光 口2.1.3反应的标准摩尔吉布斯函数变 的计算及应用 1.标准摩尔吉布斯函数变的计算△,G9 0 (I)利用物质的△rGm 规定在标准条件下由指定的单质生成 1mol纯物质B时反应的吉布斯函数变,叫 做该物质的标准摩尔生成吉布斯函数。 2025/2/15 下页 25
2025/2/15 25 2.1 化学反应的方向和吉布斯函数变 2.1.3 反应的标准摩尔吉布斯函数变 的计算及应用 1. 标准摩尔吉布斯函数变的计算 △rGm Ө (1)利用物质的△fGm Ө 规定在标准条件下由指定的单质生成 1mol纯物质B时反应的吉布斯函数变,叫 做该物质的标准摩尔生成吉布斯函数