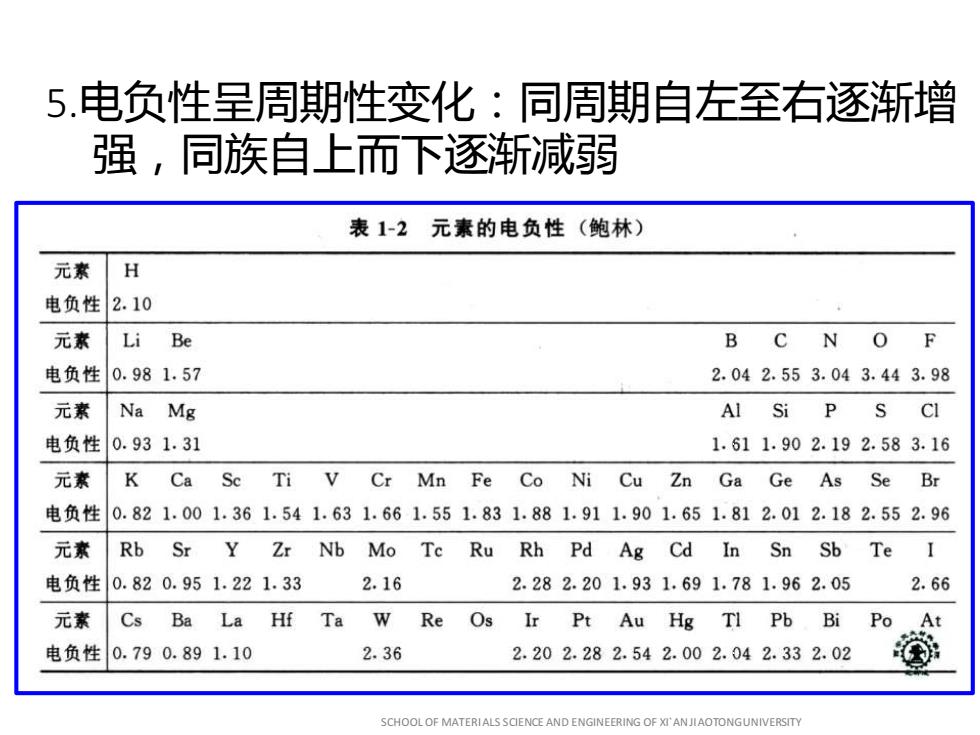
5.电负性呈周期性变化:同周期自左至右逐渐增 强,同族自上而下逐渐减弱 表1-2元素的电负性(鲍林) 元素 H 电负性2.10 元素 Li Be BCN O F 电负性0.981.57 2.042.553.043.443.98 元素 Na Mg Al Si P S CI 电负性0.931.31 1.611.902.192.583.16 元素 K Ca Se Ti Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br 电负性0.821.001.361.541.631.661.551.831.881.911.901.651.812.012.182.552.96 元素 Rb Sr Y Zr Nb Mo Te Ru Rh Pd Ag Cd In Sn Sb Te 电负性0.820.951.221.33 2.16 2.282.201.931.691.781.962.05 2.66 元素 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At 电负性0.790.891.10 2.36 2.202.282.542.002.042.332.02 SCHOOL OF MATERIALS SCIENCE AND ENGINEERING OF XI'ANJIAOTONGUNIVERSITY
5.电负性呈周期性变化:同周期自左至右逐渐增 强,同族自上而下逐渐减弱 SCHOOL OF MATERIALS SCIENCE AND ENGINEERING OF XI`AN JIAOTONGUNIVERSITY

第二节 原子间的键合 THE ATOMIC BOND 金属键 离子键 一次键 共价键 范德瓦尔斯力 二次键 氢键 SCHOOL OF MATERIALS SCIENCE AND ENGINEERING OF XI ANJIAOTONGUNIVERSITY
第二节 原子间的键合 THE ATOMIC BOND SCHOOL OF MATERIALS SCIENCE AND ENGINEERING OF XI`AN JIAOTONGUNIVERSITY 金属键 离子键 共价键 范德瓦尔斯力 氢键 一次键 二次键
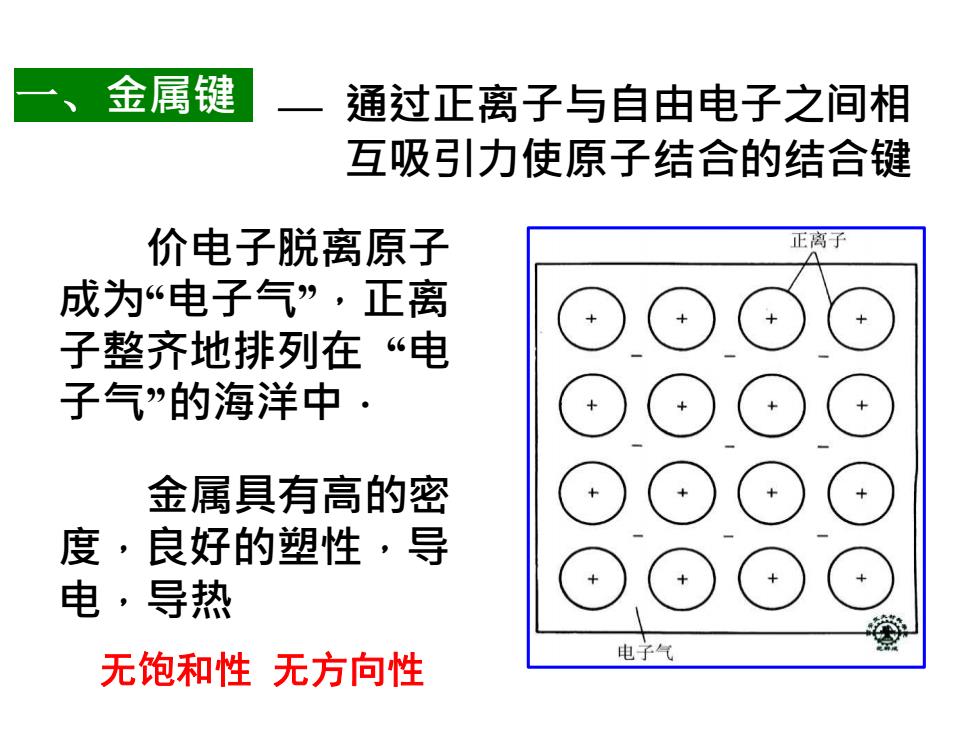
一、金属键 通过正离子与自由电子之间相 互吸引力使原子结合的结合键 价电子脱离原子 正离子 成为“电子气”,正离 子整齐地排列在“电 子气”的海洋中· 金属具有高的密 度,良好的塑性,导 电,导热 无饱和性无方向性 电子气
— 通过正离子与自由电子之间相 互吸引力使原子结合的结合键 一、金属键 价电子脱离原子 成为“电子气”,正离 子整齐地排列在 “电 子气”的海洋中. 金属具有高的密 度,良好的塑性,导 电,导热 THE END无饱和性 无方向性

二.离子键 通过正负离子间相互吸引力使原 子结合的结合键 … 例如,NaCI、MgO.. 无饱和性 对于NaCl: 无方向性 Na:1s22s22p63s1 CI:1s22s22p63s23p5 Na原子失去一个外层电子·变成正离 子,带正电 C原子得到一个外层电子,变成负离 子,带负电 THE END
二.离子键 — 通过正负离子间相互吸引力使原 子结合的结合键. 子,带负电 例如,NaCl、MgO… 对于 NaCl: Na:1s22s22p63s1 Cl:1s 22s 22p63s23p5 Na 原子失去一个外层电子,变成正离 子,带正电 Cl 原子得到一个外层电子,变成负离 THE END 无饱和性 无方向性